Ujjpercek ischaemia, nephroangiosclerosis és gócszegmenses glomerulosclerosis: a genetikai trombofília az egyedülálló magyarázat?
1 Klinikai és Kísérleti Orvostudományi Osztály, Nefrológiai Iskola, Pisai Egyetem, Via Paradisa 2, 56100 Pisa, Olaszország
Absztrakt
Esetismertetés. 53 éves, esszenciális magas vérnyomásban és nonnephrotikus proteinuriában (1,3 gr/24 óra) normál vesefunkciójú (eGFR-MDRD 123 ml/perc/1,73 m 2) férfit vettek fel a nephrológiai osztályra; a vese biopsziája FSGS-t mutatott; két évvel később a beteg fekélyt és iszkémiás gangrénát mutatott a IV és V jobb oldali ujjhegyén; genetikai elemzés kimutatta a C677T (heterozigóta C677T/1298AC, normál homociszteinértékű) metilenetetrahidrofolát-reduktáz gének polimorfizmusát, valamint a protrombin G20210A gén és a plazminogén aktivátor inhibitor-1 4G/5G 675 mutációit, értékének enyhe növekedésével. A biopsziától eltelt öt év után a 24 órás proteinuria még mindig körülbelül 1–3,3 g/meghal; a vesefunkció továbbra is normális volt (eGFR 107 ml/perc/1,73 m 2). Ezek az adatok ellentétesek az elsődleges FSGS korábbi diagnózisával. Feltételezzük, hogy a genetikai trombofília megmagyarázhatja betegünk összes klinikai tünetét. Következtetések. A trombofília génjeinek változását ki kell zárni azoknál a betegeknél, akiknél az „elsődleges” FSGS bioptikus diagnózisa van, különösen, ha klinikailag atipikus.
1.Háttér
A fokális szegmentális glomerulosclerosis a léziók hisztopatológiai mintázata, ahol a „gócos” a glomerulusok kisebbségének, a „szegmentális” pedig a glomeruláris kapilláris csomó egy részének bevonására utal, amelyet a podocyták sérülése okoz. Klinikailag proteinuria manifesztálódik, amely nefrotikus szindrómává és végső stádiumú veseelégtelenséggé válhat. Néhány klinikai és analitikai adat rendkívül hasznos lehet az FSGS primer vagy genetikai formáinak megkülönböztetésében a hiperszűrő típusoktól.
A proteinuria lassú növekedése, valamint a hypoalbuminemia és az ödéma hiánya még a proteinuria jelenlétében is nagyon jellemző a hiperszűrő FSGS-re. Ez ellentétben áll a nephrotikus szindróma gyors megjelenésével és az elsődleges típusok veseműködésének gyors csökkenésével.
Az FSGS különböző típusai közötti különbségtétel döntő fontosságú, mivel kezelésük gyökeresen eltérő.
A trombotikus mikroangiopathia az adaptív FSGS ritka oka az örökletes thrombophilia miatt. A cikk célja azt javasolni, hogy az öröklött trombofíliát vegyék figyelembe a másodlagos FSGS lehetséges okaként.
2. Esetismertetés
Ebben a cikkben beszámolunk egy 53 éves olasz férfi (testtömeg 85 kg, magasság 1,85 m, BMI 24,8 kg/m 2) szív- és érrendszeri és vesebetegségek (apa, hipertóniában és krónikus betegségben szenvedő) ismeretében. vesebetegség, akut miokardiális infarktus miatt 55 évesen elhunyt). A beteget 42 éves korában közepesen esszenciális hipertóniában diagnosztizálták, és kalciumcsatorna-blokkolók (5 mg amlodipin) és ACEI (5 mg ramipril) kombinált terápiával kezelték. 47 éves korában a laboratóriumi analízis normál vesefunkciójú hypercholesterinaemiát (összkoleszterin 270 mg/dl) és nemfrotikus proteinuriát (1,3 gr/24 óra) mutatott (szérum kreatinin 0,8 mg/dl, eGFR-MDRD 123 ml/perc/1,73 m 2 ).
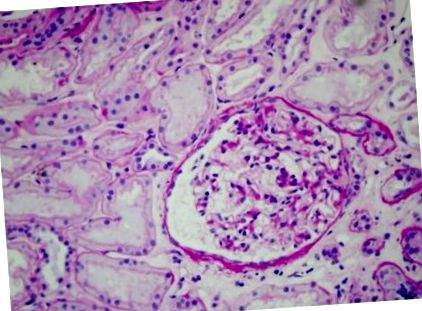
A beteget nefrológiai osztályra vitték, ahol vese biopsziát végeztek. A biopsziás anyag 19 glomerulust tartalmazott: a globális glomeruláris szklerózist és a limfociták infiltrációját négy glomerulusban mutatták ki (1. ábra), a szegmentális szklerózis kis területeit két másik glomerulusban találták, a fennmaradó 13 glomerulus pedig csak kisebb rendellenességeket mutatott (2. ábra). A tubuláris atrófia, az interstitialis fibrosis és az interlobularis sclerosis ritka jeleit is észrevették. Az immunfluoreszcencia vizsgálat nem mutatta ki az IgA, IgG, IgM, C1q, C3, k és lambda fragmensek lerakódását. A végső diagnózis az elsődleges fokális és a szegmentális glomerulosclerosis (FSGS) volt. E diagnózis szerint a beteget étrendi nátrium-korlátozással, vérnyomáscsökkentő gyógyszerekkel (5 mg ramipril és 100 mg lozartán) és nagy dózisú glükokortikoid terápiával (metilprednizolon 1000 mg ev havonta egyszer három hónapig), majd 1 mg/kg prednizonnal kezelték. meghal (75 mg), az adag fokozatos csökkentésével 6 hónapig. A kezelés végén a proteinuria az 1. ábra volt
A genetikai elemzések alapján a beteget 6 hónapig 400 mcg/mólos folsavval és 800 mg pentoxifillinnel kezelték, és hosszú távon 100 mg/dózisú acetilszalicilsavval kezelték. Az 53 éves beteget idén nephrológiai klinikánkon értékelték. Az artériás vérnyomás 140/90 Hgmm az 5 mg ramipril és a 100 mg lozartán kezelésében; a vizeletvizsgálat pH-ja 5,5, a vizelet gravitációja 1020, a fehérjék 30 mg/dl; A 24 órás vizeletfehérje kiválasztódása 1–1,3 g/meghaladó tartományban van; a vesefunkció továbbra is normális (sCr 0,76 mg/dl és eGFR 107 ml/perc/1,73 m 2). Ezek az adatok ellentétesek az elsődleges FSGS korábbi diagnózisával. A cikk célja örökletes thrombophilia felvetése a másodlagos FSGS lehetséges okaként ebben a betegben.
3. Megbeszélés
A protrombin (PT) (G20210A) [2], a metilén-tetrahidrofolát-reduktáz (MTHFR) (C677T) [1] és az V. faktor Leiden (G1691A) [3] jól ismert genetikai kockázati tényező a vénás trombózisban, míg szerepük a az artériás trombózis még tisztázandó. Az V. faktor Leiden, a PT G20210A és az MTHFR C677T polimorfizmusok növelik a szívinfarktus, az ischaemiás stroke és a perifériás érrendszeri betegségek kockázatát, különösen a fiatalabb betegek és a nők körében [4]. Kimutatták azt is, hogy a G20210A PT allél örökletes kockázati tényezőt jelent az akut koszorúér szindrómában [5]. Ezenkívül esszenciális hipertóniában, homozigóta C677TT vagy kétszeresen heterozigóta C677CT/1298AC genotípusokban szenvedő betegek hajlamosak hypertoniás nephrosclerosis és krónikus veseelégtelenség kialakulására [6]. A krónikus glomerulonephritisben gyakori nephrosclerosis intraglomeruláris véralvadással határozható meg, például a trombotikus mikroangiopathiában [7].
A hajdani egyetlen betegségnek tekintett fókuszi szegmentális glomerulosclerosis ma a klinikai-kóros szindrómák csoportjaként tekinthető közös glomeruláris elváltozásra, amelyet a podocitákra irányított különféle sértések közvetítenek. Általában az FSGS-t elsődleges, idiopátiás formának minősítik, keringő permeabilitási tényezők közvetítik, vagy másodlagos formának. A fokális szegmentális glomeruloszklerózis általában több olyan beállítást eredményez, amelyet a glomeruláris hipertrófia hiperfiltrációja közvetít (pl. Oligonephronia, egyoldalú vese agenesis vagy reflux nephropathia vagy szisztémás betegség, például súlyos elhízás, magas vérnyomás, diabetes mellitus, vasculitis, lupus és glomeruláris trombitis okozta hegesedés). mikroangiopathia antifoszfolipid szindrómában [8]). Egyéb ismert okok a HIV-fertőzés, a heroin nephropathia, az interferon és a pamidronato gyógyszerek.
Az elsődleges FSGS-t súlyos proteinuria és a vesefunkció károsodásának progressziója jellemzi, míg a másodlagos formák, különösen az adaptív forma, csak szerény proteinuriát, a vesekárosodás enyhe progresszióját és jobb prognózist mutatnak [9].
Fontos megkülönböztetni az elsődleges és a másodlagos FSGS-t, mert a kezelés gyökeresen eltérő. A másodlagos FSGS-kezelés angiotenzin-gátlásból áll, mint idiopátiás formában immunszuppresszív terápia.
Betegünk klinikai adatai valóban összhangban vannak a krónikus glomerulonephritis és az örökletes thrombophilia közötti összefüggésről szóló közelmúltbeli jelentéssel. Örökölt trombofília a 17 beteg közül nyolcban (47%) fordult elő idiopátiás vese érrendszeri betegségben: PT G20210A mutációt, V faktor Leiden mutációt és homozigozitást találtak az MTHFR C677T polimorfizmus szempontjából. Megjegyezzük, hogy 7/11 betegnél a bioptikus diagnózis FSGS volt. Egyik betegnek sem volt nephrotikus szindróma, és vesefunkciójuk mérsékelten csökkent (átlagosan 45 ml/perc/1,73 m 2, 15 és 79 ml/perc/1,73 m 2 közötti eGFR-t számoltunk) [10, 11].
4. Konklúziók
Összességében a szakirodalmi jelentések és a páciensünk adatai arra utalnak, hogy a hivatkozott örökletes trombofil faktorok hipertóniás nephrosclerosis okozta trombotikus mikroangiopátián és glomeruláris hegeken keresztül vezethetnek FSGS-hez; ráadásul ez az esettanulmány megerősíti, hogy a jelentett mutáció vese érrendszeri szklerózishoz vezethet.
rövidítések listája
| MDRD: | Módosított étrend vesebetegségben |
| PT: | Protrombin |
| MTHFR: | Metilenetetrahidrofolát-reduktáz |
| FSGS: | Focalis szegmentális glomerulosclerosis. |
Beleegyezés
Az esettanulmány és a kísérő képek közzétételéhez írásos tájékoztatáson alapuló beleegyezést kaptak a betegtől. Az írásbeli hozzájárulás egy példánya megtekinthető a folyóirat szerkesztője számára
Érdekkonfliktus
A szerzők kijelentik, hogy nincsenek összeférhetetlenségük.
Hivatkozások
- A. S. Hussein, „Három protrombotikus polimorfizmus magas prevalenciája a palesztinok körében: V faktor G1691A, II faktor G20210A és metilén-tetrahidrofolát reduktáz C677T” Journal of Thrombosis és Thrombolysis, köt. 34, pp. 383–387, 2012. Megtekintés: Publisher Site | Google ösztöndíjas
- F. Bhaijee, B. Jordan, D. J. Pepper, R. Leacock és W. A. Rock Jr. „Vénás trombózis mind a heterozigóta V faktor Leiden (R507Q), mind a II. Faktor (G20210A) mutációival” Klinikai laboratóriumi tudomány, köt. 25, pp. 199–205, 2012. Megtekintés: Google Scholar
- Y. Saemundsson, S. V. Sveinsdottir, H. Svantesson és P. J. Svensson: „V Leiden homozigóta faktor és kettős heterozigozitás a V faktor Leiden és protrombin mutáció esetén” Journal of Thrombosis és Thrombolysis, köt. 36, pp. 324–331, 2013. Megtekintés: Google Scholar
- F. Burzotta, K. Paciaroni, V. De Stefano és mtsai: „A G20210A protrombin génváltozatának megnövekedett prevalenciája akut koszorúér szindrómákban, metabolikus vagy szerzett rizikófaktorok nélkül vagy korlátozott mértékű betegséggel” European Heart Journal, köt. 23. sz. 1, pp. 2002. január 30–30. Megtekintés: Kiadói webhely | Google ösztöndíjas
- R. J. Kim és R. C. Becker, „Társulás az V. faktor Leiden, a protrombin G20210A és a metiletenetrahidrofolát reduktáz C677T mutációi és az artériás keringési rendszer eseményei között: a közzétett tanulmányok metaanalízise” American Heart Journal, köt. 146. sz. 6. o. 948–957, 2003. Megtekintés: Kiadói webhely | Google ösztöndíjas
- P. Koupepidou, C. Deltas, T. C. Christofides, Y. Athanasiou, I. Zouvani és A. Pierides: "A ciprusi betegek MTHFR 677TT és 677CT/1298AC genotípusai hajlamosak lehetnek a magas vérnyomású nephrosclerosisra és a krónikus veseelégtelenségre." Nemzetközi angiológia, köt. 24. sz. 3, pp. 287–294, 2005. Megtekintés: Google Scholar
- N. L. Kozlovskaia, L. A. Bobrova, V. V. Shkarupo, V. A. Varshavskiǐ és N. G. Miroshnichenko: „A vesebetegségek klinikomorfológiai jellemzői genetikai trombofíliában szenvedő betegeknél”. Terapevticheskiǐ Arkhiv, köt. 81. sz. 8. o. 2009. 30–36. Megtekintés: Google Scholar
- M. C. Amigo, „Vese-diszézis antifoszfolipid szindrómában” Észak-Amerika Reumatikus Klinikái, köt. 32. o. 509–522, 2006. Megtekintés: Google Scholar
- J. A. Velosa, K. Holley, V. E. Torres és K. P. Offord: „A proteinuria jelentősége a vesefunkció kimenetelén fokális szegmentális glomerulosclerosisban szenvedő betegeknél” Mayo Klinika Proceedings, köt. 58. sz. 9. o. 568–577, 1983. Megtekintés: Google Scholar
- R. L. Goforth, H. Rennke és S. Sethi: „A vese vaszkuláris szklerózis örökletes thrombophiliákkal társul”. Vese International, köt. 70. sz. 4, pp. 743–750, 2006. Megtekintés: Publisher Site | Google ösztöndíjas
- M. Bochud, M. Burnier és I. Guessous: „A három legfontosabb farmakogenomikai és személyre szabott gyógyászati alkalmazás a vesepatofiziológia és a szív- és érrendszeri orvoslás összefüggésében”. Jelenlegi farmakogenomika és személyre szabott orvoslás, köt. 9. sz. 4, pp. 299–322, 2011. Megtekintés: Google Scholar
- Focal segmental glomerulosclerosis MedlinePlus Medical Encyclopedia
- Teljes cikk Fókusszegmenses glomeruloszklerózis nagy kétoldalú tünetmentes páciensnél
- Kután mastocytosis Genetikai és Ritka Betegségek Információs Központja (GARD) - egy NCATS program
- Genetikai és epigenetikai variáció, de nem diéta, formálja a spermium metilómát - ScienceDirect
- A szaporodás szempontjából releváns elhízás genetikai és környezeti eredete - ScienceDirect